

以AI助力新药研发及精准医学,商汤科技公布多项重磅研究成果
source link: https://www.0-tech.com/archives/57351
Go to the source link to view the article. You can view the picture content, updated content and better typesetting reading experience. If the link is broken, please click the button below to view the snapshot at that time.

以AI助力新药研发及精准医学,商汤科技公布多项重磅研究成果
2021年8月4日,全球领先的人工智能平台公司商汤科技SenseTime公布了以原创AI技术赋能新药研发和精准医学的多项最新重磅研究成果,覆盖药物发现、临床前研究、临床试验、新药上市后等多个药物研发环节,旨在通过AI技术加速新药研究和上市流程,缩短新药研发周期、降低药品研发成本、提高新药研发成功率。目前,相关成果已发表在《自然精准肿瘤学》(Nature Precision Oncology)、《生物信息学》(Bioinformatics)、国际人工智能联合会议(IJCAI)等国际顶尖期刊及会议上,同时开源相关代码,为医药行业的基础研究和创新提供前沿的突破思路。
商汤科技副总裁、研究院副院长张少霆表示,“新药研发是关系着人类生命健康的事业,是一项艰巨且风险极高的工作,需要多学科之间的相互合作。依托商汤科技沉淀多年的原创技术能力,商汤智慧健康首次以AI赋能新药研发,希望全面深入发掘化合物、蛋白、细胞系和临床大数据中的潜在规律,为加速新药研发进程提供精准的依据,并逐步覆盖新药研发多个环节,帮助药企和相关研发机构降低药物研发风险、提高效益,加速新药的研发和落地,为提升人类健康水平贡献力量。”
药物发现:自主学习蛋白相互作用及其分类,辅助药物作用靶点定位
作为构成细胞的基本有机物,蛋白质分子及其之间的相互作用是细胞实现各项复杂功能的基础。因此,基于蛋白相互作用(protein-protein interactions,简称PPI)构建蛋白关系网络,可帮助分析疾病发生时的分子作用机制,从而帮助研究人员发现和理解药物作用靶点,推动新药研发。然而,以实验研究为主的传统PPI研究方法不仅耗时长,且难以有效分析PPI的具体分类。通过计算机模拟虽然可以快速为实验室研究提供候选PPI、加速实验效率,但是现有方法在遇到训练集中未包含的蛋白数据时仍会出现性能损失,不能很好地泛化到未知的蛋白及PPI。这也对不断发现的新蛋白质及其PPI、以及由此产生的潜在新靶点的分析提出了巨大挑战。
商汤智慧健康团队基于大量研究,在发布于IJCAI的《Learning Unknown from Correlations: Graph Neural Network for Inter-novel-protein Interaction Prediction》一文中提出了一种新的衡量指标(metrics),通过新的数据划分方式,有效衡量模型在跨数据集、未知蛋白上的性能效果;同时还提出了一种新的建模方法(methodology),创新性地训练了一套能够学习蛋白间关联关系的GNN(图神经网络)模型,实现了更稳定的跨数据集表现,从而实现了在未知PPI预测上的更优性能。在行业通用的公开数据集上进行的跨数据集实验中,商汤提出的新方法比现有方法的预测精度提高了36%。这两大创新方案可以在新药研发过程中,更好地帮助药物作用靶点的发现、理解和选择。
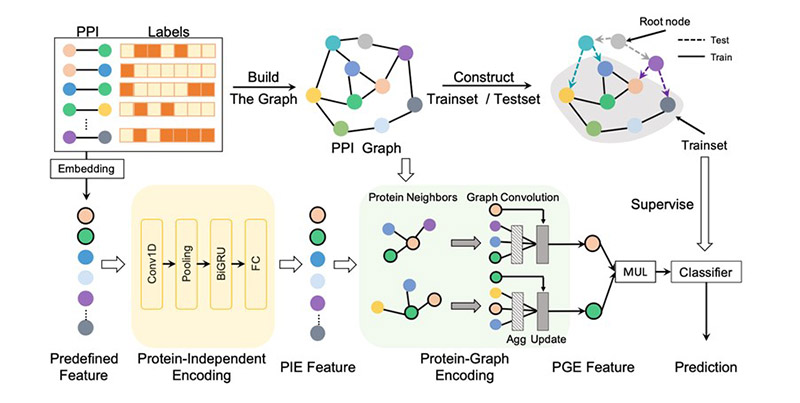 高鲁棒性的基于GNN的PPI分析框架
高鲁棒性的基于GNN的PPI分析框架 临床前研究:高效细胞系数据处理,准确预测癌症药物反应
在新药研发的临床前实验阶段,对目标疾病的药物反应进行准确预测是最重要、也最具挑战性的任务,尤其是在癌症治疗领域。临床前的实验主要涉及使用计算模型和相关细胞组织在实验室环境下的各项分析测试,为后续的人体临床试验垫定基础。近年来,高通量基因测序技术的快速发展极大地推动了基于细胞系的癌症药物反应研究。然而,鉴于癌症致病机理和药物作用机制的复杂性,传统方法仍不能有效抓取药物的化学结构特征,并充分整合基因组、转录组等多种组学信息,限制了药物反应预测准确率的进一步提升。
在发布于《生物信息学》的《DeepCDR: a hybrid graph convolutional network for predicting cancer drug response》研究中,商汤智慧健康团队首次将GCN(图卷积网络)应用在癌症药物反应研究领域,提出了一种全新的混合图卷积网络模型DeepCDR。该模型可以自动挖掘和建立药物化学结构特征,并能高效处理细胞系里的基因组学、转录组学、表观基因组学等多元组学数据,实现了对抗癌药物反应的精准预测。在覆盖238种药物和561种细胞系的公开数据集上,该模型将预测精度指标(皮尔森相关系数)从0.780提升到了0.923,为抗癌药物在临床前的实验室环境下测试药物敏感性、以及寻找肿瘤中调节药物反应的新基因等提供了更加精准高效的研究工具。
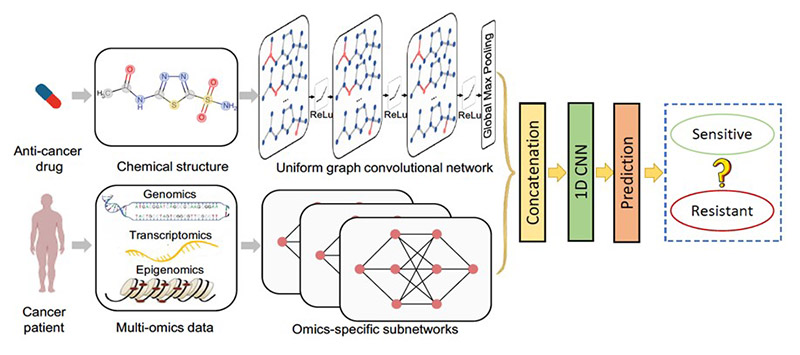 基于混合图卷积网络的基因多组学和药物化合物在癌症药物疗效评估分析
基于混合图卷积网络的基因多组学和药物化合物在癌症药物疗效评估分析 临床研究:基于病理图像预测癌症亚型,为降低亚型评估成本提供全新思路
随着精准医疗技术的不断发展,针对某种癌症亚型或特定基因突变进行个性化治疗的靶向药物逐渐成为癌症药物治疗的主要手段。新的抗癌药物的研发也大都集中在这一领域。目前,为了确定患者所患的具体癌症亚型,需要对患者的病灶组织进行基因测序,通过不同的基因突变情况进行分类,检测的成本十分昂贵。
商汤智慧医疗团队提出了一种全新的思路,利用深度学习技术挖掘数字病理图像中的细胞特征信息,从而判断组织的基因突变类别和相关生物信号通路信息。利用这一方法,商汤智慧医疗团队成功的预测了肺癌、乳腺癌、肝癌中的多个重要基因突变特征,其中最好的预测性能指标(AUC)达到0.852。这一项研究为确定患者癌症亚型提供了一种全新的思路和方法,未来可能将大幅度降低确定癌症亚型的成本,从而造福癌症患者。
 基于病理细胞图像的TP53基因突变预测
基于病理细胞图像的TP53基因突变预测 新药上市后:助推老药新用,AI预测药物新适应症
鉴于新药研发超长的研发周期和巨大的投入,上市后的老药新用可以基于已知的化合物信息,以较低的成本和较短的周期进入临床。然而,由于已上市的药物数量相对有限,同时缺乏有效的药物与新适应症的筛选模型,导致目前市面上老药新用的成功案例很少。只有做到充分挖掘药物、疾病、蛋白之间的多维关系,才能为预测新适应症提供更可靠的分析。
对此,商汤智慧健康团队创造性地训练了一套覆盖药物、疾病、蛋白多个领域间相互作用复杂关系的大规模GCN网络模型,从而精准预测药物与疾病之间的关系。该模型无需任何人工干预便可自主学习各关键信息间的关系,实现预测过程的全自动化以及对未知药物适应症的有效预测。在公开的repoDB小分子药物重定向的数据集上,相比目前使用的机器学习方法公开的最好结果,此方法的预测结果取得了更好的成绩,使相关科研团队的预测结果性能指标(AUC)提升了8%(0.792→0.857)。目前,利用这项研究结果预测出的某种已经上市的心脏疾病药物对于乳腺癌治疗的潜在有效性,已经被临床文献所证实。未来,商汤智慧健康团队希望利用这种方法,助力更高效的药物新适应症筛选过程,推动老药新用的临床进展。
基于药物、蛋白、疾病关系建模的药物重定向分析框架
回首过往,新冠疫情加速了全球医药行业的创新步伐。与此同时,国内今年来的药品带量采购、药品管理法修订等新政也助推了行业变革的到来,国内外各大药企纷纷加大新药研发力度。展望未来,人工智能技术也将为推动医药行业的创新发展发挥积极作用。凭借领先的原创AI技术,商汤科技此次公布的四大研究成果将为新药研发的多个环节奠定创新基础,助力医药行业智能化升级,进一步推动“医疗新基建”的长远发展。目前,商汤也已经与国内外多家顶级药企和基因检测公司建立商业合作,共同利用AI技术加速新药、基因等前沿创新方向的研发,加快成果转化,从而造福人类健康事业。
Recommend
About Joyk
Aggregate valuable and interesting links.
Joyk means Joy of geeK